
produkt introduksjon
| Pyridin Grunnleggende informasjon |
| Kjemisk struktur Kjemiske egenskaper Produksjoner Bruker Giftighetsinformasjon Farer Referanser |
| Produktnavn: | Pyridin |
| Synonymer: | pyridinkarboksylsyre,2-(4,5-dihydro-4-metyl-4-(1-metyletyl)-5-okso-1h-imidazol{ {9}}yl)-5-metyl;pyridinkarboksylsyre,2-(4,5-dihydro-4-metyl-4-(1-metyletyl){{ 17}}okso-1h-imidazol-2-yl)-5-metyl,monoammoniumsalt;Rcra avfallsnummer U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;FEMA NUMMER 2966;azabenzen |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| MW: | 79.1 |
| EINECS: | 203-809-9 |
| Produkt kategorier: | Ravfargede glassflasker;NMR;Løsemiddelflasker;Løsemiddel etter bruk;Løsemiddel etter type;Løsemiddelemballasjealternativer;Bioteknologiske løsemidlerLøsemidler;Løsemiddelflasker;Løsemidler;Sikkert/forsegling? Flasker; Spektrofotometrisk kvalitet; Spektrofotometriske løsemidler; Spektroskopiløsningsmidler (IR; UV/Vis); Organostannes; Tributylstanny; Kjemi; PS; Alpha Sort; Flyktige stoffer/ Halvflyktige stoffer; Ravglassflasker; ReagentPlus(R) Solvent Grade Plu-produkter; ;ACS Grade Solvents;CHROMASOLV PlusCHROMASOLV Solvents (HPLC, LC-MS);CHROMASOLV(R) Plus;LC-MS Plus and Gradient;Alphabetic;P;PU - PZ;Pyridin;Organohalides;Boronic ester;Organoborons;Organosilane;ACS Grade -Bulkløsningsmidler;ACS-kvalitetsløsningsmidler;Karbonstålbokser med NPT-tråder;Returnerbare beholderløsningsmidler;ACS- og reagenskvalitetsløsninger;ReagentPlus;ReagentPlus-løsningsmiddelkvalitetsprodukter;Bioteknologiske løsemidler;Sure/forsegle flasker;ACS-kvalitet;Analytisk reagenser for generell bruk; ;Analytisk/kromatografi;Multikompendial;Puriss pa;Puriss pa ACS;PVC-belagte flasker;aluminiumsflasker;CHROMASOLV Plus;kromatografireagenser &;HPLC &;HPLC Plus Grade Solvents (CHROMASOLV);HPLC/UHPLC Solvents (UPVCHROM); Løsningsmidler (CHROMASOLV);ACS-klasse løsemidler;Karbonstålbokser med NPT-tråder;Semi-Bulk løsemidler;Halogenert;Fluorert;Byggeklosser;Borsyre;Karboksy;Alkoksy;Analytiske reagenser for generell bruk;OP, Puriss pa;Puriss pa;OP , Puriss pa ACS;Puriss pa ACS;Aluminiumsflasker;Alfabetiske lister;Smaker og dufter;OP;Spectrophotometric Grade Solvents;Spectrophotometric GradeSolvents;PVC-belagte flasker;ReagentPlus(R) Solvent Grade ProductsSolvents;Anhydrous Grade Solvents;VannfriSolvents{0Solvents; };bc0001 |
| Mol fil: | 110-86-1.mol |
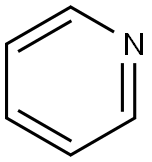 |
|
| Pyridin kjemiske egenskaper |
| Smeltepunkt | -42 grad (opplyst) |
| Kokepunkt | 115 grader (opplyst) |
| tetthet | 0.978 g/ml ved 25 grader (lit.) |
| damptetthet | 2,72 (mot luft) |
| damptrykk | 23,8 mm Hg (25 grader) |
| brytningsindeks | n20/D 1.509 (lit.) |
| FEMA | 2966|PYRIDIN |
| Fp | 68 grader F |
| lagringstemp. | Lagre ved +5 grader til +30 grader . |
| løselighet | H2O: i samsvar |
| pka | 5,25 (ved 25 grader) |
| form | Væske |
| farge | fargeløs |
| Lukt | Kvalmende lukt kan påvises ved 0.23 til 1.9 ppm (gjennomsnittlig=0.66 ppm) |
| Relativ polaritet | 0.302 |
| PH | 8,81 (H2O, 20 grader) |
| eksplosjonsgrense | 12.4% |
| Luktterskel | 0.063 ppm |
| Lukt Type | fiskeaktig |
| Vannløselighet | Blandbare |
| Frysepunktet | -42 grad |
| λmaks | λ: 305 nm Amax: 1.00 λ: 315 nm Amax: 0.15 λ: 335 nm Amax: 0,02 λ: {{0}} nm Amax: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Henrys lovkonstant | 18,4 ved 30 grader (headspace-GC, Chaintreau et al., 1995) |
| Eksponeringsgrenser | TLV-TWA 5 ppm (-15 mg/m3) (ACGIH, MSHA og OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Dielektrisk konstant | 12,5 (20 grader) |
| Stabilitet: | Stabil. Brannfarlig. Uforenlig med sterke oksidasjonsmidler, sterke syrer. |
| InChIKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 0.64 ved 20 grader |
| CAS-databasereferanse | 110-86-1(CAS DataBase Reference) |
| NIST kjemireferanse | Pyridin(110-86-1) |
| IARC | 2B (Vol. 77, 119) 2019 |
| EPA stoffregistersystem | Pyridin (110-86-1) |
| Sikkerhetsinformasjon |
| Farekoder | T,N,F,Xn |
| Risikoerklæringer | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Sikkerhetserklæringer | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | FN 1282 3/PG 2 |
| WGK Tyskland | 2 |
| RTECS | UR8400000 |
| F | 3-10 |
| Selvantennelsestemperatur | 482 grader |
| Merknad om fare | Meget brannfarlig/skadelig |
| TSCA | Ja |
| HS kode | 2933 31 00 |
| Fareklasse | 3 |
| Pakkegruppe | II |
| Data om farlige stoffer | 110-86-1(data om farlige stoffer) |
| Giftighet | LD50 oralt hos rotter: 1,58 g/kg (Smyth) |
| IDLA | 1,000 ppm |
| HMS-datablad informasjon |
| Forsørger | Språk |
|---|---|
| SigmaAldrich | Engelsk |
| ACROS | Engelsk |
| ALFA | Engelsk |
| Pyridinbruk og syntese |
| Kjemisk struktur | Pyridin er en basisk heterosyklisk organisk forbindelse med den kjemiske formelen C5H5N. Det er strukturelt beslektet med benzen, med en metingruppe (=CH−) erstattet av et nitrogenatom. Pyridinringen forekommer i mange viktige forbindelser, inkludert aziner og vitaminene niacin og pyridoksin.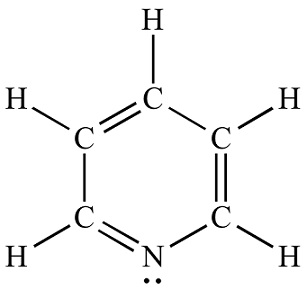 Pyridine Lewis struktur |
| Kjemiske egenskaper | Pyridin er en fargeløs brennbar væske med en sterk og ubehagelig fiskelignende lukt. Pyridin |
| Produksjoner | 2.1 Separasjon fra tjære Pyridinbaser er en bestanddel av tjære. De ble isolert fra kulltjære eller kullgass før syntetiske produksjonsprosesser ble etablert. Mengdene som finnes i kulltjære og kullgass er små, og pyridinbasene isolert fra dem er en blanding av mange komponenter. Således, med noen få unntak, var isolering av rene pyridinbaser kostbart. I dag produseres nesten alle pyridinbaser ved syntese.2.2 Chichibabin syntese 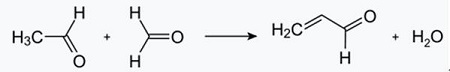 Fig. 2-1Dannelse av akrolein fra acetaldehyd og formaldehyd 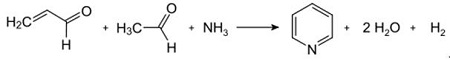 Fig. 2-2Kondensering av pyridin fra akrolein og acetaldehyd Chichibabin-pyridinsyntesen ble rapportert i 1924 og er fortsatt i bruk i industrien. Acetaldehyd og formaldehyd reagerer med ammoniakk og gir hovedsakelig pyridin. Først dannes akrolein i en Knoevenagel-kondensasjon fra acetaldehydet og formaldehydet. Det kondenseres deretter med acetaldehyd og ammoniakk til dihydropyridin, og oksideres deretter med en faststoffkatalysator til pyridin. Reaksjonen utføres vanligvis ved 350-550°C og en romhastighet på 500-1000 timer-1i nærvær av en fast syrekatalysator (f.eks. silika-aluminiumoksyd). Produktet består av en blanding av pyridin, enkle metylerte pyridiner (pikolin) og lutidin. Det gjenvunnede pyridinet separeres fra biprodukter i en flertrinnsprosess. 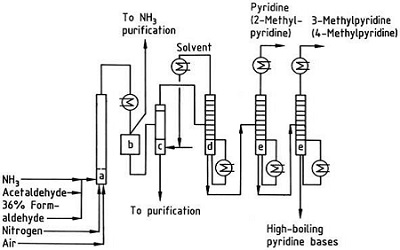 Fig. 2-3Flytskjema for pyridin- og metylpyridinproduksjon fra acetaldehyd og formaldehyd med ammoniakk. A) Reaktor; b) Samler; c) utvinning; d) Løsningsmiddeldestillasjon; e) Destillasjon 2.3 Dealkylering av alkylpyridiner Pyridin kan fremstilles ved dealkylering av alkylerte pyridiner, som oppnås som biprodukter i syntesen av andre pyridiner. Den oksidative dealkyleringen utføres enten ved bruk av luft over vanadium(V)oksidkatalysator, ved dampdealkylering på nikkelbasert katalysator, eller hydrodealkylering med en sølv- eller platinabasert katalysator. Utbytter av pyridin på opptil 93 % kan oppnås med den nikkelbaserte katalysatoren. 2.4 Syntese fra nitriler og acetylen Væskefasereaksjon av nitriler med acetylen utføres ved 120-180 ?C og 0.8-2.5 MPa i nærvær av en organokoboltkatalysator og gir 2-substituerte pyridiner : 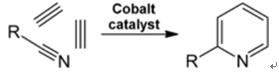 Fig. 2-4Syntese av 2-metylpyridin fra nitriler og acetylen Trimeriseringen av en del av et nitrilmolekyl og to deler acetylen til pyridin kalles Bönnemann-syklisering. Når du bruker acetonitril som nitril, oppnås 2-metylpyridin, som kan dealkyleres til pyridin. 2.5 Syntese fra akrylonitril og ketoner 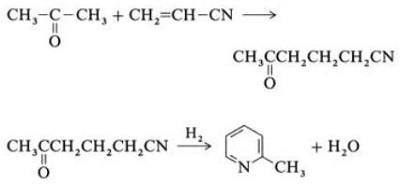 Fig. 2-5Syntese av 2-metylpyridin fra akrylnitril og aceton Syntese fra akrylnitril og aceton gir 2-metylpyridin selektivt, som kan dealkyleres til pyridin. Først skjer reaksjonen av akrylnitril og aceton, katalysert av et primært alifatisk amin som isopropylamin og en svak syre som benzosyre, i væskefasen ved 180 °C og 2,2 MPa for å gi 5-oksoheksanenitril, med 91 % selektivitet. Akrylnitrilomdannelsen er 86%. Deretter blir ringslutning og dehydrering av det opprinnelige produktet utført i gassfasen i nærvær av hydrogen over en palladium-, nikkel- eller koboltholdig katalysator ved 240°C for å gi 2-metylpyridin i 84 % utbytte. 2.6 Syntese fra Dinitriles I en dampfasereaksjon over en nikkelholdig katalysator i nærvær av hydrogen, gir 2-metylglutaronitril 3-metylpiperidin, som deretter gjennomgår dehydrogenering over palladium-alumina for å gi 3-metylpyridin. Og 3-metylpyridin kan også dealkyleres til pyridin. 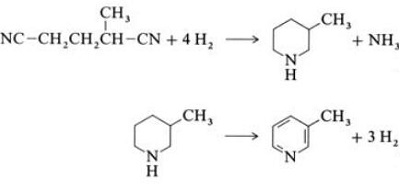 Fig. 2-6Syntese av 2-metylpyridin fra Dinitriles En ett-trinns gassfasereaksjon over en palladiumholdig katalysator er rapportert å gi 3-metylpyridin i 50 % utbytte. 2.7 Biosyntese Flere pyridinderivater spiller viktige roller i biologiske systemer. Mens biosyntesen ikke er fullt ut forstått, forekommer nikotinsyre (vitamin B3) i noen bakterier, sopp og pattedyr. Pattedyr syntetiserer nikotinsyre gjennom oksidasjon av aminosyren tryptofan, hvor et mellomprodukt, anilin, danner et pyridinderivat, kynurenin. Tvert imot produserer bakteriene Mycobacterium tuberculosis og Escherichia coli nikotinsyre ved kondensering av glyceraldehyd 3-fosfat og asparaginsyre. 2.8 Andre metoder Etylen og ammoniakk reagerer i nærvær av en palladiumkomplekskatalysator for å gi 2-metylpyridin og MEP. Pyridin kan fremstilles fra cyklopentadien ved ammoksidasjon, eller fra 2-pentennitril ved cyklisering og dehydrogenering. Furfurylalkohol eller furfural reagerer med ammoniakk i gassfasen og gir pyridin. 2-Metylpyridin fremstilles også fra anilin. |
| Bruker | 3.1 Løsemiddel Pyridin(110-86-1) er et polart, basisk, lavreaktivt løsningsmiddel, spesielt for dehydrokloreringsreaksjoner og ekstraksjon av antibiotika. I eliminasjonsreaksjonen fungerer pyridin som basen for elimineringsreaksjonen og binder det resulterende hydrogenhalogenidet for å danne et pyridiniumsalt. Ved forestringer og acyleringer aktiverer pyridin karboksylsyrehalogenidene eller anhydridene. 3.2 Medisiner Pyridins kjemiske struktur kan finnes i ulike medisiner som syntetiseres delvis takket være pyridin. Et eksempel er en medisin kalt esomeprazol, det generiske navnet på Nexium. Dette er en medisin som brukes til å behandle GERD, eller gastroøsofageal reflukssykdom. Et annet eksempel på en pyridinholdig medisin er loratadin, mer kjent under merkenavnet Claritin. Loratadin hjelper i behandlingen av allergier. 3.3 Sprøytemidler Hovedbruken av pyridin er som en forløper til ugressmidlene paraquat og diquat. Det første syntesetrinnet av insektmiddelet klorpyrifos består av klorering av pyridin. Pyridin er også startforbindelsen for fremstilling av pyritionbaserte soppdrepende midler. Cetylpyridinium og laurylpyridinium, som kan produseres fra pyridin med en Zincke-reaksjon, brukes som antiseptisk i munn- og tannpleieprodukter. Pyridin angripes lett av alkyleringsmidler for å gi N-alkylpyridiniumsalter. Et eksempel er cetylpyridiniumklorid.  Fig 3-1 Syntese av paraquat 3.4 Syntese av piperidin Piperidin, en grunnleggende heterosyklus av nitrogen, er en viktig syntetisk byggestein. Piperidiner produseres ved hydrogenering av pyridin med en nikkel-, kobolt- eller rutheniumbasert katalysator ved forhøyede temperaturer. C5H5N + 3 H2 → C5H10NH3,5 Ligand og Lewis base Pyridin er mye brukt som en ligand i koordinasjonskjemi. Som en ligand av metallkompleks kan den lett erstattes av en sterkere Lewis-base, som kan brukes i katalyse av polymerisasjons- og hydrogeneringsreaksjoner. Etter at reaksjonen er fullført, kan pyridinligand erstattet under reaksjonen gjenopprettes igjen. Pyridin brukes også som base i kondensasjonsreaksjoner. Som base kan pyridin brukes som Karl Fischer-reagens, men det erstattes vanligvis av alternativer med en mer behagelig lukt, som imidazol. 3.6 Andre Bortsett fra ovennevnte bruksområder, brukes Pyridine også til å produsere polykarbonatharpikser, vitaminer, matsmak, maling, fargestoffer, gummiprodukter, lim og vanntetting for tekstiler. Pyridin tilsettes etanol for å gjøre det uegnet til drikking. Det brukes også i in vitro-syntese av DNA. |
| Informasjon om toksisitet | 4.1 Toksisitetsnivå Lav toksisitet 4.2 Akutt toksisitet LD501580mg/kg (store mus, oral); 1121mg/kg (kanin, gjennom huden); inhalert av menneske 25mg/m3×20 min, irritasjon av bindehinne og øvre luftveisslimhinne. Subakutt og kronisk toksisitet: inhalert av store mus 32,3mg/m3×7 timer/dag x5 dager/uke x6 måneder, økning i levervekt; inhalert av mennesker 20-40mg/m3 (langsiktig), nerveskade, ustabil gange, digitale skjelvinger, lavt blodtrykk, oversvette, sporadiske lever- og nyreskader. |
| Farer | 5.1 Helsefarer Pyridin er ekstremt giftig ved svelging og innånding. Damp er tyngre enn luft. dens forbrenning produserer giftige nitrogenoksider. Pyridin er svært brannfarlig (flammepunktet er bare 17 ºC). Pyridin kan også ha nevrotoksiske og genotoksiske effekter. 5.2 Brannfare Atferd i brann: Damp er tyngre enn luft og kan reise betydelige avstander til antennelseskilden og tilbakeslag. |
| Referanser |
https://en.wikipedia.org/wiki/Pyridin#Occurrence http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/chemistry/pyridine_formula/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Pyridine https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_EN.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridine#section=Topp http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/pyridine Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Pyridine and Pyridine Derivatives", Ullmanns Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_399 |
| Kjemiske egenskaper | Pyridin, er en lett gul eller fargeløs væske; hygroskopisk; ubehagelig lukt; brennende smak; svakt alkalisk i reaksjonen; løselig i vann, alkohol, eter, benzen og fettoljer; egenvekt, 0.978; selvantennelsestemperatur, 482 grader. Pyridin, et tertiært amin, er en noe sterkere base enn anilin og danner lett kvaternære ammoniumsalter. |
| Kjemiske egenskaper | Pyridin er en svak base (pKa{{0}}.25); en 0,2 M løsning har en pH på 8,5 (HSDB 1988). Dens karbonatomer deaktiveres mot elektrofil substitusjon. Dette gjelder spesielt i sure medier, hvor det dannes salter ved nitrogenet. Den gjennomgår imidlertid lett nukleofil substitusjon, fortrinnsvis ved C-2 og også i C-4-posisjon (Jori et al 1983). Som et tertiært amin, reagerer pyridin med alkyleringsmidler for å danne kvaternære salter (Santodonato et al 1985). På grunn av sin reduserte kapasitet til å donere elektroner, er den mer motstandsdyktig mot oksidasjon enn benzen. Oksidasjon med peroksysyrer danner pyridin-N-oksid som deretter er i stand til å gjennomgå elektrofil substitusjon (Jori et al 1983). Pyridin reagerer voldsomt med en rekke forbindelser, inkludert salpetersyre, svovelsyre, maleinsyreanhydrid, perkromat, beta-propiolakton og klorsulfonsyre. Termisk nedbrytning kan frigjøre cyanider (Gehring 1983). Både pyridiniumionet og pyridin i seg selv reduseres lett til den kommersielt viktige forbindelsen, piperidin (Jori et al 1983). |
| Fysiske egenskaper | Klar, fargeløs til blekgul, brennbar væske med en skarp, gjennomtrengende, kvalmende fiskelignende lukt. Luktterskelkonsentrasjoner i vann og luft var 2 ppm (Buttery et al., 1988) og 21 ppbv(Leonardos et al., 1969), henholdsvis. Deteksjon av luktterskelkonsentrasjoner på 0,74 mg/m3(2,3 ppmv) og 6 mg/m3(1,9 ppmv) ble eksperimentelt bestemt av henholdsvis Katz og Talbert (1930) og Dravnieks (1974). Cometto-Mu?iz og Cain (1990) rapporterte en gjennomsnittlig terskelkonsentrasjon for nasal skarphet på 1275 ppmv. |
| Hendelse | Pyridin ble oppdaget av Anderson i kulltjære i 1846 (Windholz et al 1983). Den finnes i tobakksrøyk (Vohl og Eulenberg 1871; Lehmann 1909) og brent kaffe (Bertrand og Weisweiller 1913). Pyridin finnes i treolje og i bladene og røttene til Atropa belladonna (HSDB 1988), og er også en komponent i kreosotolje (Krone et al 1986). I naturen er pyridin og dets derivater ofte funnet som komponenter av alkaloider, vitaminer og koenzymer. |
| Bruker | Pyridin brukes som løsemiddel i malings- og gummiindustrien; som et mellomprodukt i fargestoffer og legemidler; for denaturering av alkohol; og som et reagens for cyanidanalyse. Det forekommer i kulltjære. |
| Bruker | Pyridin brukes direkte i denaturering av alkohol (ACGIH 1986; HSDB 1989; NSC 1978) og som løsemiddel i maling og gummipreparering (ACGIH 1986; HSDB 1989; NSC 1978) og i forskningslaboratorier for funksjoner som utvinning av plantehormoner ( Santodonato et al. 1985). Halvparten av pyridinet som produseres i dag, brukes som mellomprodukt ved fremstilling av ulike insektmidler og ugressmidler for landbruksapplikasjoner (ACGIH 1986; Harper et al. 1985; Santodonato et al. 1985). Omtrent 20 % går til produksjon av piperidin (Harper et al. 1985; Santodonato et al. 1985) som er kommersielt viktig ved fremstilling av kjemikalier som brukes i gummivulkanisering og landbruk (NSC 1978). Pyridin brukes også som et mellomprodukt i fremstillingen av medikamenter (antihistaminer, steroider, sulfa-type og andre antibakterielle midler), fargestoffer, vannavstøtende midler og polykarbonatharpikser (ACGIH 1986; Harper et al. 1985; NSC 1978; Santodonato et al. 1985). Pyridin er også godkjent av Food and Drug Administration (FDA) for bruk som smaksstoff ved tilberedning av matvarer (Harper et al. 1985; HSDB 1989). |
| Definisjon | ChEBI: Pyridin er en azaaren som omfatter en benzenkjerne der en -CH-gruppe er erstattet med et nitrogenatom. Det er hovedforbindelsen til klassen pyridiner. Molekylene har en sekskantet plan ring og er isoelektroniske med benzen. Pyridin er et eksempel på en aromatisk heterosyklisk forbindelse, med elektronene i karbon-karbon pi-bindingene og det ensomme paret av nitrogen delokalisert over atomringen. Forbindelsen utvinnes fra kulltjære og brukes som løsemiddel og som råstoff for organisk syntese. |
| Produksjonsmetoder | Pyridin produseres fra gassene som oppnås ved koksing av kull og ved direkte syntese. Den lette oljefraksjonen av kulltjære behandles med svovelsyre for å produsere vannløselige pyridinsalter og deretter gjenvinnes pyridinbasene fra den vandige fasen med natriumhydroksid eller ammoniakk (Jori et al 1983). Størstedelen av amerikansk produksjon er gjennom syntetiske midler. Denne prosessen bruker en dampfasereaksjon av acetaldehyd, formaldehyd og ammoniakk, som gir en blanding av pyridin og 3-metylpyridin (Santodonato et al 1985). Produktforholdet avhenger av de relative mengder av acetaldehyd og formaldehyd. Tilsatt metanol øker utbyttet. Den amerikanske produksjonen av pyridin ble estimert til 32 til 47 millioner pund i 1975 (Reinhardt og Brittelli 1981). Pyridin er kommersielt tilgjengelig i tekniske, 2 graders og 1 graders karakterer, de to sistnevnte refererer til deres kokeområde. Store urenheter er høyerekokende homologer, som pikoliner, lutidiner og kollidiner, som er mono-, di- og trimetylpyridiner (Santodonato et al 1985; Jori et al 1983). |
| Forberedelse | Pyridin produseres enten ved isolering fra naturlige kilder som kull, eller gjennom kjemisk syntese (HSDB 1989). Pyridin produseres ved fraksjonert destillasjon av kull-tjærerester (HSDB 1989; NSC 1978; Santodonato et al. 1985) hvor 1 tonn kull produserer 0.07-0.21 pounds av pyridinbaser av hvor 57 % er pyridin (Santodonato et al, 1985). Syntetisk produsert pyridin er for tiden den viktigste kilden til pyridin for kommersiell bruk (Santodonato et al. 1985). Små mengder pyridin syntetiseres fra acetaldehyd, formaldehyd og ammoniakk med en fluidisert silika-aluminiumoksyd-katalysator, etterfulgt av fraksjonering for å isolere pyridinet (Harper et al. 1985; HSDB 1989; NSC 1978). Pyridin produseres fra naturlige kilder av Crowley Tar Products fra Stow, Ohio og Oklahoma City, Oklahoma (Harper et al. 1985; HSDB 1989; SRI 1986, 1987, 1988). Pyridin produseres syntetisk av to selskaper, Nepera Chemical Co. i Harriman, New York og Reilly Tar and Chemical Corporation i Indianapolis, Indiana (Harper et al. 1985; SRI 1986, 1987, 1988). |
| Aromaterskelverdier | Deteksjon: 0.079 til 790 ppb; gjenkjenning: 7,9 til 40 ppm |
| Generell beskrivelse | En klar fargeløs til lysegul væske med en gjennomtrengende kvalmende lukt. Tetthet 0,978 g/cm3. Flammepunkt 68 grader F. Damp er tyngre enn luft. Giftig ved svelging og innånding. Forbrenning produserer giftige oksider av nitrogen. |
| Luft- og vannreaksjoner | Meget brannfarlig. Løselig i vann. |
| Reaktivitetsprofil | Azabenzen er en base. Reagerer eksotermt med syrer. Under fremstilling av et kompleks av azabenzen med kromtrioksid, en syre, ble andelen kromtrioksid økt. Oppvarming fra denne syre-base-reaksjonen førte til en eksplosjon og brann [MCA Case History 1284 1967]. En 0,1 % løsning av azabenzen (eller annet tertiært amin) i maleinsyreanhydrid ved 185 grader gir en eksoterm dekomponering med rask utvikling av gass [Chem Eng. Nyheter 42(8); 41 1964]. Blanding av azabenzen i like molare porsjoner med noen av følgende stoffer i en lukket beholder førte til at temperaturen og trykket økte: klorsulfonsyre, salpetersyre (70%), oleum, svovelsyre (96%) eller propiolakton [NFPA 1991]. Kombinasjonen av jod, azabenzen, svoveltrioksid og formamid utviklet en gass over trykk etter flere måneder. Dette oppsto fra den langsomme dannelsen av svovelsyre fra eksternt vann, eller fra dehydrering av formamidet til hydrogencyanid. Etylenoksid og SO2 kan reagere voldsomt i azabenzenløsning med trykksetting dersom etylenoksid er i overkant (Nolan, 1983, Case History 51). |
| Fare | Brannfarlig, farlig brannfare, eksplosjonsgrenser i luft 1,8–12,4 %. Giftig ved svelging og innånding. Hudirriterende, lever- og nyreskade. Tvilsomt kreftfremkallende. |
| Helsefare | Den akutte toksisiteten til pyridin er lav. Innånding forårsaker irritasjon av luftveiene og kan påvirke sentralnervesystemet, forårsake hodepine, kvalme, oppkast, svimmelhet og nervøsitet. Pyridin irriterer øynene og huden og absorberes lett, noe som fører til systemiske effekter. Inntak av pyridin kan føre til lever- og nyreskade. Pyridin forårsaker lukttretthet, og lukten gir ikke tilstrekkelig advarsel om tilstedeværelsen av skadelige konsentrasjoner. Pyridin er ikke funnet å være kreftfremkallende eller å vise reproduksjons- eller utviklingstoksisitet hos mennesker. Kronisk eksponering for pyridin kan føre til skade på leveren, nyrene og sentralnervesystemet. |
| Helsefare | De toksiske effektene av pyridin inkluderer hodepine, svimmelhet, nervøsitet, kvalme, søvnløshet, hyppig vannlating og magesmerter. Symptomene var forbigående, oppstod hos mennesker fra subakutt eksponering for pyridindamper ved ca. 125 ppm i 4 timer om dagen i 1–2 uker (Reinhardt) og Brittelli 1981). Målorganene for pyridintoksisitet er sentralnervesystemet, leveren, nyrene, mage-tarmkanalen og huden. Eksponeringsveiene er innånding av damper, og inntak og absorpsjon av væsken gjennom huden. Alvorlige helsefarer kan oppstå ved kronisk innånding, som kan forårsake nyre- og leverskade, og stimulering av benmarg for å øke produksjonen av blodplater. Eksponering på lavt nivå for 10 ppm kan gi kroniske forgiftningseffekter på sentralnervesystemet. Inntak av væsken kan gi de samme symptomene som nevnt ovenfor. Hudkontakt kan forårsake dermatitt. Damp er irriterende for øyne, nese og lunger. På grunn av den sterke ubehagelige lukten er det alltid tilstrekkelig advarsel mot overeksponering. En konsentrasjon på 10 ppm er upassende for mennesker. LCLO-verdi, innånding (rotter): 4000 ppm/4 timer LD50-verdi, oral (mus): 1500 mg/kg. Huh og medarbeidere (1986) har undersøkt effekten av glycyrrhetinic acid på pyridintoksisitet hos mus. Forbehandling med glycyrrhetinsyre reduserte depresjon av sentralnervesystemet og dødelighet hos dyr indusert av pyridin. Slik forbehandling reduserte aktiviteten til enzymet serumtransaminase markant og økte aktiviteten til hepatisk mikrosomal anilinhydroksylase [9012-90-0], et pyridinmetaboliserende enzym. |
| Brennbarhet og eksplosjonsevne | Pyridin er en svært brannfarlig væske (NFPA-klassifisering=3), og dampen kan bevege seg over en betydelig avstand og "glimme tilbake". Pyridindamp danner eksplosive blandinger med luft i konsentrasjoner på 1,8 til 12,4 % (volum). Karbondioksid eller tørrkjemikalier skal brukes til pyridinbrann. |
| Industriell bruk | Pyridin er et godt løsemiddel for et stort antall forbindelser, både organiske og uorganiske (Windholz et al 1983). Omtrent 50 % av pyridin som brukes i USA er til produksjon av landbrukskjemikalier, slik som ugressmidlene paraquat, diquat og triclopyr og insektmiddelet klorpyrifos. Andre bruksområder er i produksjonen av piperidin; fremstilling av legemidler, slik som steroider, vitaminer og antihistaminer; og som løsemiddel. Bruk av løsemidler finnes i både den farmasøytiske og polykarbonatharpiksindustrien. Det er spesielt nyttig som løsningsmiddel i prosesser der HC1 utvikles (Santodonato et al 1985). Mindre bruksområder for pyridin er for denaturering av alkohol- og frostvæskeblandinger, som fargehjelp i tekstiler og som smaksstoff (Jori et al 1983; Furia 1968; HSDB 1988). |
| Kontaktallergener | Pyridin (usubstituert pyridin) og dets derivat (substituerte pyridiner) er mye brukt i kjemi. Pyridin er et løsemiddel som brukes for mange organiske forbindelser og vannfrie metalliske saltkjemikalier. Inneholdt i Karl Fischer-reagens, induserte det kontakteksem hos en laboratorietekniker. Det er ikke observert kryssfølsomhet mellom de forskjellige stoffene. |
| Sikkerhetsprofil | Gift intraperitoneal. Moderat giftig ved svelging, hudkontakt, intravenøs og subkutan vei. Lett giftig ved innånding. Et hud- og alvorlig øyeirriterende middel. Mutasjonsdata rapportert. Kan forårsake depresjon i sentralnervesystemet, gastrointestinale forstyrrelser og lever- og nyreskader. En brennbar væske og farlig brannfare når den utsettes for varme, flamme eller oksidasjonsmidler. Alvorlig eksplosjonsfare i form av damp når den utsettes for flamme eller gnist. Reagerer voldsomt med klorsulfonsyre, kromtrioksid, dinitrogentetraoksid, HNO3, oleum, perkromater, ppropiolakton, AgClO4, H2SO4. Glødende reaksjon med fluor. Reagerer for å danne pyrofore eller eksplosive produkter med bromtrifluorid, trifluormetylhypofluoritt. Blandinger med formamid + jod + svoveltrioksid er lagringsfarer, og frigjør karbondioksid og svovelsyre. Uforenlig med oksiderende materialer. Reagerer med maleinsyreanhydrid (over 150 grader) og utvikler karbondioksid. For å bekjempe brann, bruk alkoholskum. Ved oppvarming til nedbrytning avgir den svært giftig røyk av NOx. |
| Potensiell eksponering | Pyridin brukes som løsemiddel i kjemisk industri og som denatureringsmiddel for etylalkohol; som et mellomprodukt i produksjonen av plantevernmidler; innen farmasøytiske produkter; i produksjon av maling, eksplosiver, fargestoffer, gummi, vitaminer, sulfa-medisiner; og desinfeksjonsmidler. |
| Kreftfremkallende egenskaper | Pyridin var ikke kreftfremkallende i flere kroniske subkutane studier. F344-rotter ble gitt pyridin oralt i drikkevann i doser på 0, 7, 14 eller 33 mg/kg i 2 år. Den høyeste dosen ga en reduksjon i kroppsvekter og vannforbruk. Økt renal tubulær adenom eller karsinom og tubulær hyperplasi ble observert hos menn ved 33 mg/kg. Økt mononukleær celleleukemi ble observert hos hunner ved 14 og 33 mg/kg, noe som ble ansett som tvetydig når det gjelder forholdet til pyridineksponering, siden dette er et vanlig funn hos denne rottestammen. Konsentrasjonsrelatert ikke-neoplastisk endring i leveren ble sett ved 33 mg/kg. Wistar-hannrotter ble behandlet på lignende måte med doser på 0, 8, 17 eller 36 mg/kg i 2 år. Redusert overlevelse og kroppsvekt ble sett ved 17 og 36 mg/kg. Økte testikkelcelleadenomer ble sett ved 36 mg/kg. Ingen endringer i overlevelse eller neoplasmerater i annet vev, inkludert nyrene, ble rapportert, selv om økt nefropati og hepatisk sentrilobulær degenerasjon/nekrose ble observert hos noen pyridinbehandlede rotter. |
| Kilde | Pyridin forekommer naturlig i poteter, anabasis, henbaneblader, peppermynte (0 til 1 ppb), teblader og tobakksblader (Duke, 1992). Identifisert som en av 140 flyktige bestanddeler i brukte soyaoljer samlet fra et prosessanlegg som stekte ulike biff-, kylling- og kalvekjøttprodukter (Takeoka et al., 1996). |
| Miljøskjebne | Biologisk.Heukelekian og Rand (1955) rapporterte en 5-d BOD-verdi på 1,31 g/g som er 58,7 % av ThOD-verdien på 2,23 g/g. En Nocardia sp. isolert fra jord var i stand til å transformere pyridin, i nærvær av semikarbazid, til et mellomprodukt identifisert som ravsyresemialdehyd (Shukla og Kaul, 1986). 1,4-Dihydropyridin, glutarsyredialdehyd, glutarsyresemialdehyd og glutarsyre ble identifisert som mellomprodukter når pyridin ble degradert av Nocardia-stamme Z1 (Watson og Cain, 1975). Fotolytisk.Bestråling av en vandig løsning ved 50 grader i 24 timer resulterte i et 23,06 % utbytte av karbondioksid (Knoevenagel og Himmelreich, 1976). Kjemisk/fysisk.Gassfasereaksjonen av ozon med pyridin i syntetisk luft ved 23 grader ga et nitreert salt med formelen: [C6H5NH]+NO3 - (Atkinson et al., 1987). Ozonering av pyridin i vandige løsninger ved 25 grader ble studert med og uten tilsetning av tert-butylalkohol (20 mM) som radikalfjerner. Med tert-butylalkohol ga ozonering av pyridin hovedsakelig pyridin-N-oksid (80 % utbytte), som var meget stabil mot ozon. Uten tert-butylalkohol spaltes den heterosykliske ringen raskt og danner ammoniakk, nitrat og amidforbindelsen N-formyloksaminsyre (Andreozzi et al., 1991). |
| Metabolisme | Pyridin absorberes gjennom mage-tarmkanalen, hud og lunger og elimineres via urin, avføring, hud og lunger, både som metabolitter og som moderforbindelse (Jori et al 1983). Opptak av vev øker med dose og eliminasjonen er bifasisk (Zharikov og Titov 1982; HSDB 1988). Elimineringen er rask og det ser ikke ut til å være noen vevsakkumulering (Jori et al 1983). Observasjonen av His (1887) av urinutskillelsen av Af-metylpyridin fra pyridindoserte dyr var det første eksemplet på Af-metylering. Kjente urinmetabolitter av pyridin hos pattedyr inkluderer nå pyridin-N-oksid, N-metylpyridin, 4-pyridon, 2-pyridon og 3-hydroksypyridin. Noen metabolitter gjenstår fortsatt å identifisere (Damani et al 1982). De relative mengder av metabolittene er svært avhengig av art og dose (Gorrod og Damani 1980). For eksempel har rotten vist seg å skille ut 70 % av en dose på 1 mg/kg i urinen i løpet av de første 24 timene etter dosering, men dette tallet synker til bare 5,8 % for en dose på 500 mg/kg (D'Souza et al. al 1980). Selv om urinutskillelse av pyridin og dets metabolitter ser ut til å være en hovedvei for eliminering, er ikke-urinutskillelse ikke blitt grundig studert (Santodonato et al 1985). Hos kaniner har pyridin-N-metyltransferaseaktiviteten vist seg å være høyest i lungecytosol, og det er funnet å bruke 5-adenosylmetionin som metyldonor (Damani et al 1986). Denne veien er mettbar i både rotte og marsvin (D'Souza et al 1980). Produktet av denne reaksjonen, N-metylpyridin, er mindre kronisk giftig, men mer akutt giftig enn pyridin (Williams 1959). Pyridin-N-oksid produseres av cytokrom P-450-systemet og aktiviteten induseres av fenobarbital eller pyridinforbehandling, men ikke av 3-metylcholanthrene (Gorrod og Damani 1979; Kaul og Novak 1987). Hos kaninen er den alkoholinduserbare (og pyridininduserbare) P-450 LM3Aser ut til å være den lave Kmisozym som katalyserer pyridin Af-oksid produksjon (Kim og Novak 1989). N-oksidasjonen av pyridin kan representere en vei for bioaktivering (Santodonato et al 1985) og denne veien blir viktigere ettersom pyridindosen økes (Damani et al 1982). |
| Oppbevaring | Pyridin bør kun brukes i områder fri for antennelseskilder, og mengder større enn 1 liter bør lagres i tett lukkede metallbeholdere i områder atskilt fra oksidasjonsmidler. |
| Shipping | UN1992 Brannfarlige væsker, giftige, nei, Fareklasse: 3; Etiketter: 3-Brannfarlig væske, 6.1-Giftige materialer, teknisk navn påkrevd. |
| Rensemetoder | Sannsynlige urenheter er H2O og aminer som pikoliner og lutidiner. Pyridin er hygroskopisk og er blandbart med H2O og organiske løsemidler. Den kan tørkes med fast KOH, NaOH, CaO, BaO eller natrium, etterfulgt av fraksjonert destillasjon. Andre metoder for tørking inkluderer henstand med Linde type 4A molekylsikter, CaH2 eller LiAlH4, azeotropisk destillasjon av H2O med toluen eller *benzen, eller behandlet med fenylmagnesiumbromid i eter, etterfulgt av fordampning av eteren og destillasjon av pyridin. En anbefalt [Lindauer Mukherjee Pure Appl Chem 27 267 1971]-metode tørker pyridin over fast KOH (20g/Kg) i 2 uker og fraksjonert destillerer supernatanten over Linde type 5A molekylsikter og fast KOH. Produktet lagres under CO2-fritt nitrogen. Pyridin kan lagres i kontakt med BaO, CaH2 eller molekylsikter. Ikke-basiske materialer kan fjernes ved å dampdestillere en løsning som inneholder 1,2 ekvivalenter 20 % H2SO4 eller 17 % HCl inntil ca. 10 % av basen er blitt overført sammen med de ikke-basiske urenhetene. Resten gjøres deretter alkalisk, og basen separeres, tørkes med NaOH og fraksjonelt destilleres. Alternativt kan pyridin behandles med oksidasjonsmidler. Således har pyridin (800 ml) blitt omrørt i 24 timer med en blanding av ceriumsulfat (20 g) og vannfri K2CO3 (15 g), deretter filtrert og fraksjonert destillert. Hurd og Simon [J Am Chem Soc 84 4519 1962] rørte pyridin (135mL), vann (2,5L) og KMnO4 (90g) i 2 timer ved 100o, ble deretter stående i 15 timer før de filtrerte av de utfelte manganoksidene. Tilsetning av fast KOH (ca. 500 g) førte til at pyridin separerte. Den ble dekantert, tilbakeløpskokt med CaO i 3 timer og destillert. Separasjon av pyridin fra noen av dets homologer kan oppnås ved krystallisering av oksalater. Pyridin utfelles som dets oksalat ved å tilsette det til den omrørte løsningen av oksalsyre i aceton. Bunnfallet filtreres, vaskes med kald aceton, og pyridin regenereres og isoleres. Andre metoder er basert på kompleksdannelse med ZnCl2 eller HgCl2. |
| Inkompatibiliteter | Voldsom reaksjon med sterke oksidasjonsmidler; sterke syrer; klorsulfonsyre; maleinsyreanhydrid; oleum jod. |
| Avfallshåndtering | Kontrollert forbrenning der nitrogenoksider fjernes fra avløpsgassen ved hjelp av skrubber, katalytiske eller termiske enheter. |
| Pyridinforberedelsesprodukter og råvarer |
| Råvarer | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIAMINOPENTAN DIHYDROKLORID |
| Forberedelsesprodukter | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Paraquat diklorid |
Populære tags: pyridin, Kina pyridin produsenter, leverandører, fabrikk
Du kommer kanskje også til å like
Sende bookingforespørsel







