
produkt introduksjon
| Hypofosforsyre Grunnleggende informasjon |
| Oversikt Kjemiske egenskaper Bruker Toksisitet FAREIDENTIFIKASJON Tilberedningsmetode Produksjonsmetode |
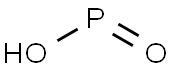
| Produktnavn: | Hypofosforsyre |
| Synonymer: | HYPOFOSFORSYRE,30%(W/V)LØSNING;HYPOFOSFORSYRE,50%(W/V)LØSNING;Hypofosforsyre: (fosfinsyre);Hypofosforsyre, 50% w/w aq. soln.;hypofosforsyre;hypofosforsyre(ætsende flytende,sur,uorganisk,nos);Hypofosforsyre,50%w/waq.soln.;HYPOFOSFORSYRELØSNING 50% VANDIG |
| CAS: | 6303-21-5 |
| MF: | HO2P |
| MW: | 63.980501 |
| EINECS: | 228-601-5 |
| Produktkategorier: | HPA;Uorganiske stoffer;6303-21-5 |
| Mol fil: | 6303-21-5.mol |
 |
|
| Hypofosforsyre Kjemiske egenskaper |
| Smeltepunkt | -25 grad |
| Kokepunkt | 108 grader (759,8513 mmHg) |
| tetthet | 1,206 g/ml ved 20 grader (lit.) |
| damptrykk | <17 mmHg ( 20 °C) |
| lagringstemp. | ingen restriksjoner. |
| løselighet | svært løselig i H2O, etanol, etyleter |
| pka | pK1 1.1. |
| form | hygroskopiske krystaller eller fargeløs oljeaktig væske |
| farge | Fargeløs |
| Vannløselighet | LØSELIG |
| Merck | 13,4894 |
| Stabilitet: | Stabil. Uforenlig med sterke baser. Reagerer voldsomt med oksidasjonsmidler, sterke baser, kvikksølv (II) nitrat og kvikksølv (II) oksid. Ikke varm opp over 100 C. |
| InChIKey | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| CAS-databasereferanse | 6303-21-5(CAS DataBase Reference) |
| NIST kjemireferanse | Hypofosforsyre(6303-21-5) |
| EPA stoffregistersystem | Fosfinsyre (6303-21-5) |
| Sikkerhetsinformasjon |
| Farekoder | C |
| Risikoerklæringer | 34 |
| Sikkerhetserklæringer | 26-36/37/39-45 |
| RIDADR | FN 3264 8/PG 3 |
| WGK Tyskland | 1 |
| RTECS | SZ6400000 |
| TSCA | Ja |
| Fareklasse | 8 |
| Pakkegruppe | II |
| HS-kode | 28111990 |
| Data om farlige stoffer | 6303-21-5(data om farlige stoffer) |
| HMS-datablad informasjon |
| Leverandør | Språk |
|---|---|
| Fosfinsyre | engelsk |
| SigmaAldrich | engelsk |
| ACROS | engelsk |
| ALFA | engelsk |
| Hypofosforsyre bruk og syntese |
| Disposisjon | Hypofosforsyre er også kjent som "hypofosfitt" Det er en fargeløs olje eller utflytende krystall, det er et viktig fint kjemisk produkt. Hovedbruken er som reduksjonsmiddel for strømløs plettering, fosfor forhindrer misfarging av harpikser, det kan også brukes i forestringsreaksjonskatalysatoren, kjølemediet, spesielt for produksjon av høyrent produkt natriumhypofosfitt. Det er flere metoder for tilberedning, den vanlige industrielle metoden for å produsere er ionebytterharpiksmetoden og elektrodialysemetoden. De kjemiske egenskapene til hypofosforsyre, bruk, toksisitet og produksjonsmetoder er redigert av andy fra Chemicalbook. (2016-12-04) |
| Kjemiske egenskaper | Det er flytende krystaller eller fargeløs olje. Smeltepunkt: 26,5 grader. Den relative tettheten (spesifikk vekt): 1,439 (fast stoff, 19 grader). Det er løselig i vann, etanol og eter, og det kan blandes i alle forhold med vann, etanol, aceton. I luften smelter den lett til sirupsaktig væske, og den vandige løsningen er sur. Hypofosforsyre er monobasisk syre, i vandig løsning, Hypofosforsyre er sterk syre, Ka=10-2 (25 grader ); den er relativt stabil ved romtemperatur; disproporsjoneringsreaksjonen kan fortsette ved 130 grader, spaltes til fosfin og fosforsyre: 2H3PO2=H3PO4+PH3 Den har sterk reduksjon, tungmetallsaltløsning kan gjenopprettes til metaller som Cu2 +, Hg2 +, Ag +, for eksempel: 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ Det er svakt oksidasjonsmiddel, det kan reduseres til fosfin, fosfin når man møter sterkt reduksjonsmiddel. |
| Bruker | 1. Hypofosforsyre brukes som reduksjonsmiddel for strømløs plettering; 2. Den kan brukes til å forhindre misfarging av fosforsyreharpiks; 3. Det brukes som esterifiseringskatalysator, kjølemediet; 4. Det brukes til å produsere hypofosfitt, natriumsalter, mangansalter, jernsalter brukes vanligvis som nærende stoffer; 5. Hypofosforsyre brukes i medisin og som reduksjonsmiddel, bestemmelse av arsen, tellur og separasjon av tantal, niob og andre reagenser. 6. Det er sterkt reduksjonsmiddel, det kan brukes til fremstilling av natriumhypofosfitt, kalsiumfosfat og annet hypofosfitt. 7. Den kan brukes til pletteringsbadet. Legemidler. reduksjonsmiddel. generelle reagenser. 8. Det er sterkt reduksjonsmiddel, det kan brukes til å lage natriumhypofosfitt, kalsiumfosfat og annet hypofosfitt. 9. Dette produktet er mye brukt som reduksjonsmiddel, Ag, Cu, Ni, Hg og andre metaller reduseres til det tilsvarende metallet, for verifisering av As, Nb, Ta og andre reagenser, kan det brukes til fremstilling av Na , K, Ca, Mn, Fe og andre typer hypofosfitt. |
| Giftighet | Det er ikke brennbart. Men når det kommer i kontakt med hull H-middelet, vil det forårsake brann. Når det møter oksidasjonsmiddel, kan voldsom reaksjon og forbrenning fortsette. Når den varmes opp for høy, kan den brytes ned til svært giftig fosfingass, eller til og med eksplodere. Det er etsende. Hypofosforsyre tilsettes ofte i brus, og fordi den ikke absorberes. Så risikoen er liten, men spesielt sterk hypofosfitt skader gastrointestinal. Ved et uhell spruter det inn i øynene eller kommer i kontakt med huden, mye vann brukes til å vaske. Produksjonsoperatører bør bruke verneklær og andre verneklær. Produksjonsutstyr skal være forseglet, verksted skal være godt ventilert. |
| FAREIDENTIFIKASJON | Faresetning: Gir alvorlige hudforbrenninger og øyeskader. Gir alvorlig øyeskade Forsiktighetsutsagn: Ikke pust inn støv/røyk/gass/tåke/damp/spray. Vask grundig etter håndtering. Bruk vernehansker og øye-/ansiktsbeskyttelse. VED SVELGING: Skyll munnen. IKKE fremkall brekninger. VED HUDKONTAKT (eller hår): Fjern/ta umiddelbart av alle forurensede klær. Skyll huden med vann/dusj. VED KONTAKT MED ØYNENE: Skyll forsiktig med vann i flere minutter. Fjern kontaktlinser, hvis tilstede og lett å gjøre. Fortsett å skylle. VED INNÅNDING: Flytt den tilskadekomne til frisk luft og la den hvile i en stilling som letter pusten. Ring umiddelbart et GIFTINFORMASJONSSENTER eller en lege. Butikk innelåst. Kast dette materialet og dets beholder til innsamlingssted for farlig avfall eller spesialavfall. |
| Forberedelsesmetode | 1. Fosfor- og bariumhydroksidløsning varmes opp, bariumsalt Ba (H2PO2) 2 • 2H2O kan genereres, svovelsyre tilsettes i hypofosforsyre bariumløsning, Ba2+ kan utfelles: Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 Hypofosforsyre kan oppnås ved å fordampe under redusert trykk og lavtemperaturkrystallisering. På grunn av i denne prosessen er løseligheten til bariumsaltet liten, så konsentrasjonen av oppnådd hypofosforsyre er ikke høy, industriprodukt bør renses ved omkrystallisering. 2. bariumoksidet (eller kalken) og løsningen av hvitt fosfor varmes sammen for å danne sekundært bariumfosfat (eller kalsium), og reagerer deretter med svovelsyre, det filtreres, konsentreres for å oppnå produkt, eller natriumhypofosfittløsningen fortsetter H- type ionebytterharpiks kan avlede produkt. Denne metoden krever en stor mengde harpiks, og harpiksregenererings- og vasketrinnet er tungvint, det koster vanligvis mer enn $ 7 per pund, det er bare egnet for små batchproduksjon og ikke egnet for store industrielle applikasjoner. 3. Hypofosforsyre fremstilles ved elektrodialysemetode, hvor elektrodialysecellen deler seg i tre deler, de er anodekammer, råmaterialekammer og katodekammer, mellomproduktet er separert av anionisk membran og kationisk membran, mellom to membraner plasseres natriumhypofosfittløsning (konsentrasjon på 100g/L~500g/L), anodekammeret er en fortynnet løsning av hypofosforsyre 5g/L, anodekammeret er fortynnet natriumhydroksidløsning (5g/L), mellom polene DC (3V~36V) føres, anode frigjør oksygen og genererer sekundært produkt av hypofosforsyre; katoden avgir hydrogen, og genererer sekundært produkt av natriumhydroksid, reaksjonstiden er 3 ~ 21 timer. Reaksjonene til anodekammer og katodekammer er som følger: anode kammer: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 katodekammer: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH Elektrodialysemetode for fremstilling Hypofosforsyre er enkel og utstyrsinvesteringen er liten, den er egnet for masseproduksjon. 4. Med utgangspunkt i natriumhypofosfitt av industriell kvalitet, fjernes Cl-, SO42-anioner som påvirker kvalitetsindikatorene til hypofosforsyre ved utfelling, tungmetallioner fjernes fra løsningen ved å danne sulfid, og deretter bruke sterk syre kationbytter harpiks for å oppnå natrium sekundært fosfat, høy renhetsgrad produkt kan oppnå. Prosessen kan produsere høyverdig sekundært fosfat, teknisk gjennomførbart, prosessen er enkel, enkel betjening, god produktkvalitet, den kan møte behovene til elektronikkindustrien, forsvarsindustrien og andre høyteknologiske felt. 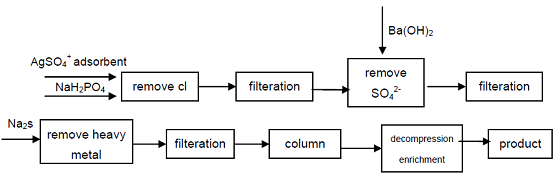 figur 1 Produksjonsprosess av hypofosforsyre fra industriell natriumhypofosfitt. 5. Ionebytterharpiksmetode: ca. 70 g kationbytterharpiks fuktet med vann pakkes inn i et glassrør med 5 mol/L saltsyre som sirkulerer ca. 15 minutter, etter grundig vask med vann, vandig høyrent vandig natriumhypofosfittløsning (15 g/ 60 ml H2O) strømmer gjennom den, harpikskolonnen vaskes først med 50 ml, deretter med 25 rnl destillert vann. Avløpssyren og vaskevæsken kombineres, den konsentreres ved fordampning i vannbad. Den konsentrerte syren plasseres i høyvakuum med P205-tørker for dehydrering, avkjøling og krystallisering, filtrering, omkrystallisering, for å oppnå hypofosforsyreprodukt. |
| Produksjonsmetode | Ionebytterharpiksmetode: legg ca. 70 g vannløselige kationbytterharpikser for å fylle i et glassrør. Sirkuler med 5 mol/L saltsyre i ca. 15 min og vask tilstrekkelig med vann. Ha en høy vandig natriumhypofosfittløsning (15 g/60 ml H2O) til å strømme gjennom harpikskolonnen, etterfulgt av å vaskes først med 50 ml vann, og deretter skylles med 25 rnl destillert vann. Avløpssyren og vaskevæskene ble kombinert og konsentrert ved fordampning på vannbad. Den konsentrerte syren sendes til høyvakuum, P205 tørketrommel for dehydrering, etterfulgt av avkjølende krystallisering, filtrering og omkrystallisering for å oppnå det ferdige produktet av hypofosforsyre. |
| Beskrivelse | Hypofosforsyre er et kraftig reduksjonsmiddel med en molekylformel H3PO2. Uorganiske kjemikere refererer til den frie syren med dette navnet, selv om dens IUPAC-navn er dihydridohydroxidooxidophosphorus, eller det akseptable navnet på fosfinsyre. Det er en fargeløs lavtsmeltende forbindelse, som er løselig i vann, dioksan og alkoholer. Formelen for hypofosforsyre er vanligvis skrevet H3PO2, men en mer beskrivende presentasjon er HOP(O)H2 som fremhever dens monoprotiske karakter. Salter avledet fra denne syren kalles fosfinater (hypofosfitter). |
| Beskrivelse | Denne syren har den generelle formelen H4P2O6 og skiller seg fra de andre oksyfosforsyrene. Den har mange særegenheter. Det dannes sammen med fosfor- og fosforsyrer, når fosfor oksideres av fuktig luft. Hvis hvitt fosfor utsettes for luft, og natriumacetat tilsettes væsken som dannes, skilles det noe uløselige natriumhypofosfatet, Na2H2P2O6·6H2O. Natriumhypofosfatmonohydratet er imidlertid svært løselig og utflytende ved -98,7 g/100 ml. |
| Kjemiske egenskaper | fargeløs væske |
| Fysiske egenskaper | Fargeløse flytende krystaller eller oljeaktig væske; sur lukt; tetthet 1,493 g/cm3;smelter ved 26,5 grader; koker ved 130 grader; svært løselig i vann, alkohol og eter; densiteten til en 50 % vandig løsning er 1,13 g/ml. |
| Bruker | Hypofosforsyre brukes først og fremst til strømløs nikkelplettering. Det er involvert i reduksjonen av arendiazoniumsalter. Det fungerer som et tilsetningsstoff i Fischer-forestringsreaksjoner. Det fungerer også som et nøytraliserende middel, antioksidant, katalysator i polymerisering og polykondensasjon, og fuktemiddel. Videre brukes det i formuleringen av legemidler, misfarging av polymerer, vannbehandling og gjenvinning av edle eller ikke-jernholdige metaller. I tillegg til dette brukes det som blekemiddel for plast, syntetiske fibre, avfargingsmiddel og til fargestabilisering ved fremstilling av kjemikalier og flere plaster. |
| Preparat | Hypofosforsyre kan fremstilles ved forskjellige metoder: 1. Kokende hvitt fosfor med kalsiumhydroksid: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 Kalsiumsaltet er løselig i vann. Behandling med svovelsyre gir hypofosforsyren: (H2PO2)2Ca + H2SÅ4 → 2H3PO2+ CaSO4 Produktblandingen filtreres for å fjerne uløselig CaS04. Den vandige løsningen av hypofosforsyre konsentreres under redusert trykk. Konsentrert barytvann kan brukes i stedet for kalsiumhydroksid.2. Ved å behandle natriumhypofosfitt, NaH2PO2 med en ionebytterharpiks. Natriumsaltet kan produseres ved å koke hvitt fosfor med en løsning av natriumhydroksid, en reaksjon som ligner på (1) ovenfor. PH3 + 2I2 + 2H2O → H3PO2+ 4HEI Metoden ovenfor kan anses som sikrere enn den som involverer oppvarming av hvit fosfor med en alkali. Hypofosforsyre må lagres under 50 grader. Det selges kommersielt som en vandig løsning i forskjellige konsentrasjoner. |
| Produksjonsmetoder | Hypofosforsyre dannes ved reaksjon av bariumhypofosfitt og svovelsyre, og filtrering av bariumsulfat. Ved å fordampe løsningen i vakuum ved 80 grader, og deretter avkjøle til 0 grader, krystalliserer hypofosforsyre. |
| Definisjon | ChEBI: En fosforoksosyre som består av en enkelt femverdig fosfor kovalent bundet via enkeltbindinger til to hydrogener og en hydroksygruppe og via en dobbeltbinding til et oksygen. Forelderen til klassen fosfinsyrer. |
| Definisjon | Et hvitt krystallinsk fast stoff. Det er en monobasisk syre som danner anion H2PO2– i vann. Natriumsaltet, og dermed syren, kan fremstilles ved å varme opp gult fosfor med natriumhydroksidløsning. Den frie syren og dens salter er kraftige reduksjonsmidler. |
| Reaksjoner | Hypofosforsyre er blandbar med vann i alle proporsjoner og en kommersiell styrke er 30 % H3PO2. Hypofosfitter brukes i medisin. Hypofosforsyre er et kraftig reduksjonsmiddel, f.eks. med kobbersulfat danner kobber(II)hydrid Cu2H2, brunt bunnfall, som utvikler hydrogengass og etterlater kobber ved oppvarming; med sølvnitrat gir finfordelt sølv; med svovelsyrling gir svovel og noe hydrogensulfid; med svovelsyre gir svovelsyre, som reagerer som ovenfor; danner mangan umiddelbart med permanganat. |
| Generell beskrivelse | Hypofosforsyre fremstår som en fargeløs oljeaktig væske eller utflytende krystaller med en sur lukt. Tetthet 1,439 g/cm3. Smeltepunkt 26,5 grader. Innånding av damper irriterer eller brenner luftveiene. Væske og damper kan irritere eller brenne øyne og hud. |
| Luft- og vannreaksjoner | Deliquescent. Vannløselig. |
| Reaktivitetsprofil | HYPOFOSFORSYRE spaltes ved oppvarming til fosforsyre og spontant brannfarlig fosfin. Oksyderes av svovelsyre med frigjøring av svoveldioksid og svovel. Reagerer eksplosivt med kvikksølv(II)oksid [Mellor, 1940, Vol. 4, 778]. Reagerer voldsomt med kvikksølv(II)nitrat [Mellor, 1940, Vol. 4, 993]. Nøytraliserer baser i eksoterme reaksjoner. |
| Fare | Brann- og eksplosjonsfare ved kontakt med oksidasjonsmidler. |
| Helsefare | GIFTIG; innånding, svelging eller hudkontakt med materiale kan forårsake alvorlig skade eller død. Kontakt med smeltet stoff kan forårsake alvorlige brannskader på hud og øyne. Unngå all hudkontakt. Effekter av kontakt eller innånding kan bli forsinket. Brann kan produsere irriterende, etsende og/eller giftige gasser. Avrenning fra brannkontroll- eller fortynningsvann kan være etsende og/eller giftig og forårsake forurensning. |
| Brannfare | Ikke-brennbart, selve stoffet brenner ikke, men kan brytes ned ved oppvarming og produsere etsende og/eller giftige gasser. Noen er oksidasjonsmidler og kan antenne brennbare stoffer (tre, papir, olje, klær osv.). Kontakt med metaller kan utvikle brennbar hydrogengass. Beholdere kan eksplodere ved oppvarming. |
| Rensemetoder | Fosforsyre er en vanlig forurensning av kommersiell 50 % hypofosforsyre. Jenkins og Jones [J Am Chem Soc 74 1353 1952] renset dette materialet ved å fordampe ca. 600 ml i en 1L kolbe ved 40o, under redusert trykk (i N2), til et volum på ca. 300 ml. Etter at løsningen var avkjølt, ble den overført til en bredmunnet Erlenmeyer-kolbe som ble tilstoppet og stående i et tørris/acetonbad i flere timer for å fryse (om nødvendig med riper i veggen). Når kolben så ble stående ved ca. 5o i 12 timer, ble ca. 30-40 % av den flytende, og ble igjen filtrert. Denne prosessen ble gjentatt, deretter ble faststoffet lagret over Mg(ClO4)2 i en vakuumekssikkator i kulde. Etterfølgende krystalliseringer fra n-butanol ved å oppløse den ved romtemperatur og deretter avkjøle i et is-saltbad ved -20o så ikke ut til å rense den ytterligere. Den frie syren danner flytende krystaller m 26,5o og er løselig i H2O og EtOH. NaH2PO2-saltet kan renses gjennom en anionbytterharpiks [Klement Z Anorg Allgem Chem 260 267 1949.] |
| Hypofosforsyrepreparater og råvarer |
| Råvarer | AMBERLITE(R) IRC-50 |
| Forberedelsesprodukter | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->Fosforsyre |
Populære tags: hypofosforsyre, Kina hypofosforsyre produsenter, leverandører, fabrikk
Et par: Kaliumbromat
Neste: Fluorborsyre
Du kommer kanskje også til å like
Sende bookingforespørsel



