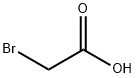
| Kjemiske egenskaper |
HVIT TIL LYSGUL KRYSTALLINK MASSE |
| Bruker |
Organisk syntese, abscisisjon av sitrusfrukt i høsting. |
| Bruker |
Bromeddiksyre brukes i organisk syntese og som alkyleringsmiddel. Det brukes også som et biokjemikalium for proteomikkforskning. Det er et viktig råstoff og mellomprodukt som brukes i organisk syntese, farmasøytiske produkter, fargestoffer og landbrukskjemikalier. |
| Bruker |
Bromeddiksyre brukes hovedsakelig tilN-terminal bromoacylering av harpiksbundne peptider.
Den kan også brukes:For å syntetisere (Z)-2-(cyklookt-4-en-1-yloksy)eddiksyre.
For å syntetisere -brom-fenylacetamid.
For å konvertere aromatiske tiosemikarbazoner til tiazolylhydrazoner.
|
| Generell beskrivelse |
Vandig løsning. |
| Luft- og vannreaksjoner |
Vannløselig. |
| Reaktivitetsprofil |
Karboksylsyrer, slik som BROMEDIKSYRE, donerer hydrogenioner hvis en base er tilstede for å akseptere dem. De reagerer på denne måten med alle baser, både organiske (for eksempel aminene) og uorganiske. Deres reaksjoner med baser, kalt "nøytraliseringer", er ledsaget av utviklingen av betydelige mengder varme. Nøytralisering mellom en syre og en base gir vann pluss et salt. Karboksylsyrer med seks eller færre karbonatomer er fritt eller moderat oppløselige i vann; de med mer enn seks karbonatomer er lett løselige i vann. Løselig karboksylsyre dissosieres til en viss grad i vann for å gi hydrogenioner. pH i oppløsninger av karboksylsyrer er derfor mindre enn 7.0. Mange uløselige karboksylsyrer reagerer raskt med vandige løsninger som inneholder en kjemisk base og løses opp ettersom nøytraliseringen genererer et løselig salt. Karboksylsyrer i vandig løsning og flytende eller smeltede karboksylsyrer kan reagere med aktive metaller og danne gassformig hydrogen og et metallsalt. Slike reaksjoner skjer i prinsippet også for faste karboksylsyrer, men er langsomme hvis den faste syren forblir tørr. Selv "uløselige" karboksylsyrer kan absorbere nok vann fra luften og oppløses tilstrekkelig i bromeddiksyre til å korrodere eller oppløse deler og beholdere av jern, stål og aluminium. Karboksylsyrer, som andre syrer, reagerer med cyanidsalter for å generere gassformig hydrogencyanid. Reaksjonen er langsommere for tørre, faste karboksylsyrer. Uløselige karboksylsyrer reagerer med løsninger av cyanider for å forårsake frigjøring av gassformig hydrogencyanid. Brannfarlige og/eller giftige gasser og varme genereres ved reaksjon av karboksylsyrer med diazoforbindelser, ditiokarbamater, isocyanater, merkaptaner, nitrider og sulfider. Karboksylsyrer, spesielt i vandig løsning, reagerer også med sulfitter, nitritter, tiosulfater (for å gi H2S og SO3), ditionitter (SO2), for å generere brennbare og/eller giftige gasser og varme. Deres reaksjon med karbonater og bikarbonater genererer en ufarlig gass (karbondioksid), men fortsatt varme. Som andre organiske forbindelser kan karboksylsyrer oksideres av sterke oksidasjonsmidler og reduseres med sterke reduksjonsmidler. Disse reaksjonene genererer varme. Et bredt utvalg av produkter er mulig. Som andre syrer kan karboksylsyrer initiere polymerisasjonsreaksjoner; som andre syrer, katalyserer de ofte (øker hastigheten på) kjemiske reaksjoner. |
| Fare |
Sterk irriterende for hud og vev. |
| Helsefare |
GIFTIG; innånding, svelging eller kontakt (hud, øyne) med damper, støv eller stoffer kan forårsake alvorlige skader, brannskader eller død. Kontakt med smeltet stoff kan forårsake alvorlige brannskader på hud og øyne. Reaksjon med vann eller fuktig luft vil frigjøre giftige, etsende eller brennbare gasser. Reaksjon med vann kan generere mye varme som vil øke konsentrasjonen av røyk i luften. Brann vil produsere irriterende, etsende og/eller giftige gasser. Avrenning fra brannkontroll- eller fortynningsvann kan være etsende og/eller giftig og forårsake forurensning. |
| Brannfare |
Brennbart materiale: kan brenne, men antennes ikke lett. Stoffet vil reagere med vann (noen voldsomt) og frigjøre brennbare, giftige eller etsende gasser og avrenning. Ved oppvarming kan damper danne eksplosive blandinger med luft: innendørs, utendørs og eksplosjonsfare i kloakk. De fleste damper er tyngre enn luft. De vil spre seg langs bakken og samles i lave eller trange områder (kloakk, kjellere, tanker). Damp kan bevege seg til antennelseskilden og blinke tilbake. Kontakt med metaller kan utvikle brennbar hydrogengass. Beholdere kan eksplodere ved oppvarming eller forurenset med vann. |
| Brennbarhet og eksplosjonsevne |
Ikke brannfarlig |
| Sikkerhetsprofil |
Gift ved svelging, intraperitoneal og intravenøs vei. Irriterende og etsende for hud og slimhinner. Mutasjonsdata rapportert. Ved oppvarming til nedbrytning avgir den giftige gasser av Br-. Se også BROMIDER. |
| Rensemetoder |
Krystalliser bromeddiksyre fra pet-eter (b 40-60o). En dietyleterløsning av den føres gjennom en aluminiumoksydkolonne, og eteren fordampes ved romtemperatur under vakuum. Det oppnås best ved destillasjon fra en Claisen (kolbe nedsenket i et oljebad) utstyrt med en isolert Vigreux-kolonne (s. 11) og fraksjonen b 108-110o/30 mm samles opp. Den er lys- og fuktfølsom. [Natelson & Gottfried Org Synth Coll Vol III 381 1955, Beilstein 2 IV 526.] LACHRYMATORY og er hudirriterende. |